Чем отличается движение молекул в газах, жидкостях и твердых телах
Согласно молекулярно-кинетической теории, все вещества могут находиться в трех состояниях: газообразном, твердом и жидком. Иногда называется четвертое состояние – плазма. При каждом из этих состояний движение молекул имеет свои особенности. Чем же отличается движение молекул в газах, жидкостях и твердых телах?
Переход из одного агрегатного состояния вещества в другое сопровождается изменением его физических свойств. Молекулы вещества в разном состоянии отличаются силой взаимодействия, характером теплового движения и расположением.
Расстояние между атомами и молекулами в газах существенно превышает размер самих частиц, а сила притяжения между ними очень слаба. По этой причине в газообразном состоянии вещество не имеет формы и постоянного объема. Газы могут легко сжиматься и расширяться. Молекулы газа движутся с очень большой скоростью, и, сталкиваясь между собой, отскакивают в разные стороны. Давление газа создается множественными ударами молекул о стенки сосуда.
Атомы и молекулы твердого тела располагаются в виде кристаллической решетки. Сила притяжения между атомами чрезвычайно велика, поэтому в данном состоянии сохраняется постоянный объем и форма вещества.
Расстояние между молекулами жидкости меньше размеров самих частиц. Сила притяжения между молекулами велика, но расположение частиц по отношению друг к другу нельзя назвать упорядоченным по всему объему. Жидкости не имеют собственной формы, но сохраняют объем. Особенностью движения молекул в жидком веществе является текучесть. Благодаря этому свойству вещество легко изменяет форму в зависимости от сосуда, сохраняя физические свойства по всем направлениям.
Выводы:
Движение молекул в газах, жидкостях и твёрдых телах
Молекулярно-кинетическая теория даёт объяснение тому, что все вещества могут находиться в трёх агрегатных состояниях: в твёрдом, жидком и газообразном. Например, лёд, вода и водяной пар. Часто плазму считают четвёртым состоянием вещества.
Агрегатные состояния вещества (от латинского aggrego – присоединяю, связываю) – состояния одного и того же вещества, переходы между которыми сопровождаются изменением его физических свойств. В этом и заключается изменение агрегатных состояний вещества.
Во всех трёх состояниях молекулы одного и того же вещества ничем не отличаются друг от друга, меняется только их расположение, характер теплового движения и силы межмолекулярного взаимодействия.
Движение молекул в газах
В газах обычно расстояние между молекулами и атомами значительно больше размеров молекул, а силы притяжения очень малы. Поэтому газы не имеют собственной формы и постоянного объёма. Газы легко сжимаются, потому что силы отталкивания на больших расстояниях также малы. Газы обладают свойством неограниченно расширяться, заполняя весь предоставленный им объём. Молекулы газа движутся с очень большими скоростями, сталкиваются между собой, отскакивают друг от друга в разные стороны. Многочисленные удары молекул о стенки сосуда создают давление газа.
Движение молекул в жидкостях
Время оседлой жизни уменьшается с повышением температуры. Расстояние между молекулами жидкости меньше размеров молекул, частицы расположены близко друг к другу, а межмолекулярное притяжение велико. Тем не менее, расположение молекул жидкости не является строго упорядоченным по всему объёму.
Жидкости, как и твёрдые тела, сохраняют свой объём, но не имеют собственной формы. Поэтому они принимают форму сосуда, в котором находятся. Жидкость обладает таким свойством, как текучесть. Благодаря этому свойству жидкость не сопротивляется изменению формы, мало сжимается, а её физические свойства одинаковы по всем направлениям внутри жидкости (изотропия жидкостей). Впервые характер молекулярного движения в жидкостях установил советский физик Яков Ильич Френкель (1894 – 1952).
Движение молекул в твёрдых телах
Молекулы и атомы твёрдого тела расположены в определённом порядке и образуют кристаллическую решётку. Такие твёрдые вещества называют кристаллическими. Атомы совершают колебательные движения около положения равновесия, а притяжение между ними очень велико. Поэтому твёрдые тела в обычных условиях сохраняют объём и имеют собственную форму.
Чем отличается движение молекул в газах, жидкостях и твердых телах?
Движение молекул в разных агрегатных состояниях вещества обусловлено связями этих молекул между собой.
Если рассматривать газы, то его молекулы движутся в беспорядочном порядке. Расстояния между ними достаточно большие, поэтому на движение друг друга они влияют слабо, так сила притяжения слишком мала.
Для жидкостей иная картина. Молекулы располагаются ближе друг к другу, тем самым на движение молекулы в жидкости непосредственное влияние оказывают соседние молекулы. Молекулы движутся, но ограниченно.
Для твердых тел притяжение между молекулами настолько большое, что они образовали кристаллическую форму. Молекулы практически не перемещаются, а колебания их происходят у равновесного положения.
Несмотря на то, что газы, жидкости и твердые тела состоят из атомов и молекул, поведение этих частиц в них различается.
Так, в газах молекулы разделены и вибрируют, свободно перемещаясь на высоких скоростях.
В жидкости расположены довольно близко друг к другу, перемещаются и скользят мимо друг друга.
В твердых телах расположены, как правило, в жестком порядке, между частицами находится мало свободного пространства. Кроме того, они обычно не перемещается с места на место.
Жидкости и твердые тела иногда называют конденсированными фазами, потому что их частицы расположены очень близко друг к другу.
Треугольник, образованный двумя верхними линиями и горизонталью, проведённой из точки К доказывает все условия, при которых диоксид углерода может быть жидким. Например, при комнатной температуре (+20°С) диоксид углерода может быть жидким в интервале давлений от 5,739 МПа (57,39 ата) до примерно 9 МПа (90 ата). При более высоких давлениях он существует в виде твёрдого вещества.
Движение молекул в физике в газах, жидкостях и твёрдых телах с примерами
Содержание:
Движение молекул:
Почему запах духов распространяется по всей комнате? Могут ли «срастись» два кусочка металла? От чего зависит скорость движения атомов и молекул? На эти и другие вопросы вы сможете ответить, прочитав этот параграф.
Тепловое движение
В соответствии с современными представлениями, атомы и молекулы, из которых состоит вещество, находятся в беспрерывном хаотическом движении. Такое движение называется тепловым.
Тепловое движение невозможно увидеть невооруженным глазом, ведь размеры молекул очень малы.
Однако существует много физических явлений, объяснить которые можно только опираясь на тот факт, что молекулы постоянно двигаются.
Определение диффузии
Бесспорным доказательством движения молекул служит физическое явление, хорошо известное вам из курса природоведения,— диффузия (от лат. diffusio — распространение, растекание).
Напомним, что диффузией называют взаимное проникновение соприкасающихся веществ друг в друга, происходящее в результате теплового (хаотического) движения молекул (атомов).
Диффузия в газах и жидкостях
Вспомните, что происходит, если где-то в комнате разлить ароматное вещество, например духи,— его запах в скором времени будет ощущаться повсюду. Это значит, что молекулы ароматного вещества, двигаясь, попадают в промежутки между молекулами воздуха, которым заполнена комната, т. е. наблюдается диффузия. Именно в результате диффузии в газах мы ощущаем запах свежеиспеченного хлеба из булочной или запах прогретой солнцем травы.
Диффузию можно наблюдать и в жидкостях. Проведем такой опыт. В прозрачный сосуд с чистой водой с помощью воронки нальем раствор медного купороса так, чтобы жидкости не смешались (рис. 2.15). Сначала мы наблюдаем резкую границу между водой и раствором медного купороса. Оставив сосуд в покое на несколько дней, мы увидим, что вся жидкость в сосуде приобрела бирюзовый цвет (рис. 2.16). Причем перемешивание жидкостей произошло без вмешательства извне. Схематически процесс диффузии изображен на рис. 2.17. Многочисленные опыты свидетельствуют, что диффузия в жидкостях протекает значительно медленнее, чем в газах. Еще медленнее происходит диффузия в твердых телах. Почему? Ответ на этот вопрос следует искать в особенностях расположения молекул газов, жидкостей и твердых тел.
Как связаны скорость движения молекул и температура
Приготовим два сосуда, как показано на рис. 2.15. Один из сосудов поставим в теплое место, второй — в холодное. Посмотрев через некоторое время на сосуды, мы убедимся, что в теплом растворе диффузия произошла намного быстрее.
В случае повышения температуры скорость диффузии в газах также увеличивается.
Зависимость скорости диффузии от температуры особенно заметна для твердых тел. Так, английский металлург Вильям Роберт Остин провел следующий опыт. Он наплавил тонкий диск золота на свинцовый цилиндр (рис. 2.18, а) и на несколько дней поместил этот цилиндр в печь, где поддерживалась температура около 400 °С. Оказалось, что золото продиф-фундировало через весь цилиндр (рис. 2.18, б); тем временем при комнатной температуре диффузия практически не наблюдалась.
Таким образом, мы выяснили, что чем выше температура вещества, тем быстрее происходит диффузия, т. е. молекулы быстрее двигаются.
Довольно сложные эксперименты показывают, что при любой температуре в веществе есть молекулы, двигающиеся довольно медленно, и молекулы, скорость которых высока. Если количество молекул вещества, имеющих высокую скорость, увеличивается, т. е. увеличивается средняя скорость молекул, то это значит, что температура вещества также увеличивается.
Диффузия в природа и ее применение в технике
Явление диффузии очень распространено в природе. Благодаря диффузии углекислый газ попадает в листву растений; кислород из воздуха — на дно водохранилищ; питательные вещества впитываются в кишечнике; кислород из легких попадает в кровь, а из крови — в ткани и т. д.
Диффузию широко применяют в технике. Одним из примеров является диффузное сваривание металлов. Куски металлов крепко прижимают друг к другу, нагревают до высокой
температуры, но ниже температуры плавления. В месте соединения происходит диффузия, и куски металлов как будто срастаются.
Атомы и молекулы, из которых состоит вещество, находятся в беспрерывном хаотическом движении. Такое движение называется тепловым, поскольку увеличение температуры вещества соответствует увеличению средней скорости движения его молекул (атомов).
Одним из доказательств движения частиц вещества является физическое явление, которое называется диффузией. Диффузия — взаимное проникновение соприкасающихся веществ друг в друга, происходящее в результате теплового хаотического движения молекул (атомов).
Движение и взаимодействие молекул
Что такое броуновское движение
Броуновское движение — хаотическое движение видимых в микроскоп малых макрочастиц, взвешенных в жидкости или газе, которое происходит под действием ударов молекул.
Это явление названо в честь шотландского ботаника Роберта Броуна (1773–1858), который первым наблюдал его в 1827 г. Рассматривая в микроскоп взвешенные в воде частички пыльцы, Броун заметил, что они непрерывно движутся, постоянно изменяя скорость.
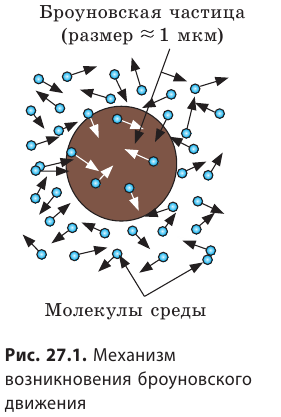
Причина броуновского движения — хаотическое движение молекул жидкости или газа. Двигаясь, молекулы среды непрерывно бомбардируют взвешенную в ней макрочастицу (рис. 27.1). Если суммарная сила ударов с одной стороны случайно окажется больше, чем с другой, то макрочастица может начать движение; потом другие толчки изменят ее скорость.
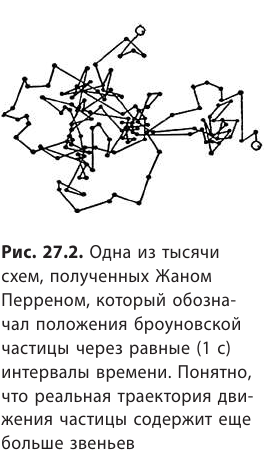
Теория броуновского движения, созданная А. Эйнштейном и польским физиком M. Смолуховским в 1905–1906 гг. и экспериментально подтвержденная французским физиком Ж. Перреном (рис. 27.2), окончательно закрепила победу атомистики.
Что такое диффузия и где ее применяют
Непрерывное хаотическое движение молекул происходит внутри любого макроскопического тела. В курсе физики 7 класса вы изучали диффузию — еще одно явление, обусловленное таким движением (от лат. diffusio — распространение, растекание).
Диффузия — процесс взаимного проникновения молекул одного вещества между молекулами другого, происходящий вследствие теплового движения молекул.
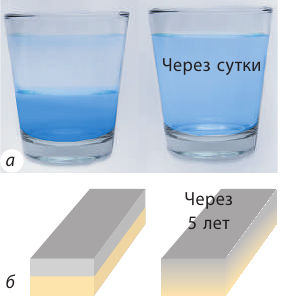
Если в стакан с водой налить подкрашенный сахарный сироп, спустя некоторое время вода в стакане окрасится и станет сладкой (рис. 27.3, а).
Рис. 27.3. Диффузия в жидкостях и твердых телах. Вследствие теплового хаотического движения молекул сироп смешался с водой в течение суток (а), две отшлифованные и прижатые друг к другу пластины свинца и золота «срослись» на 1 мм в течение 5 лет (б)
Диффузия в жидкости происходит довольно медленно, а в твердых телах она медленнее в сотни и тысячи раз (рис. 27.3). В газах диффузия протекает гораздо быстрее, чем в жидкостях, но все равно: если бы не было конвекции, запах духов распространялся бы в комнате часами. Отметим, что в любых средах скорость диффузии увеличивается с повышением температуры и давления.
Диффузные процессы очень важны для получения и обработки некоторых материалов. Диффузия в твердых телах обеспечивает соединение металлов при сварке, пайке, никелировании. С помощью диффузии поверхностный слой металлических изделий насыщают углеродом, обеспечивая их прочность (рис. 27.4).
Рис. 27.4. Цементация — процесс насыщения поверхностного слоя стали углеродом. если изготовить деталь из низкоуглеродистой стали, а затем поместить ее в высокотемпературную смесь, содержащую углерод, то благодаря диффузии поверхностный слой стали обогатится углеродом. Полученная деталь одновременно будет твердой (снаружи — крепкий чугун) и не будет разрушаться при ударных нагрузках (внутри — упругая сталь)
Разновидностью диффузии является осмос (от греч. osmos — толчок, давление) — процесс односторонней диффузии сквозь полупроницаемую перегородку (мембрану) молекул растворителя в сторону большей концентрации растворенного вещества. Например, если острым ножом отрезать дольку лимона, то сок практически не выделится; если посыпать дольку сахаром, то сок появится. Выделяясь из лимона, сок как бы стремится разбавить концентрированный раствор сахара, образовавшийся на срезе.
В природе благодаря осмосу питательные вещества и вода проникают из почвы в корни растений, из пищеварительного тракта — в организмы живых существ и непосредственно в клетки; кислород из легочных альвеол поступает в кровь и т. п. В промышленности осмос используют для очистки воды, производства напитков, получения некоторых полимеров.
Как быстро движутся молекулы
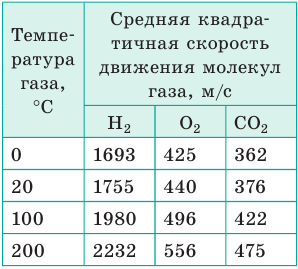
Молекулы в газах движутся очень быстро — со скоростью пули (см. таблицу), но далеко «улететь» не могут, поскольку ежесекундно испытывают более миллиарда столкновений с другими молекулами. Поэтому траектории движения молекул представляют собой сложные ломаные линии, подобные траектории движения броуновской частицы.
Обратите внимание! В веществе всегда есть молекулы, движущиеся медленно, и молекулы, скорость движения которых огромна. В результате столкновений скорости молекул непрерывно изменяются. Описать движение даже одной молекулы невозможно, да и не нужно. Важно знать, к какому результату приводит движение всей совокупности молекул данного объекта.
Как была измерена скорость движения молекул
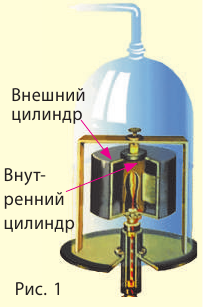
Впервые скорость движения молекул измерил немецкий физик Отто Штерн (1888–1969) в 1920 г. Для опыта Штерн изготовил устройство (см. рис. 1), состоящее из двух жестко связанных пустых цилиндров, надетых на общую ось; стенка внутреннего цилиндра имела щель. Вдоль оси была натянута металлическая нить, покрытая слоем серебра. Воздух из цилиндров был откачан. Когда по нитке пропускали ток, серебро испарялось и внутренний цилиндр заполнялся атомами Аргентума, часть которых проходила сквозь щель и оседала на внутренней стенке внешнего цилиндра. В результате напротив щели образовывалась тонкая полоска серебра (А на рис. 2).
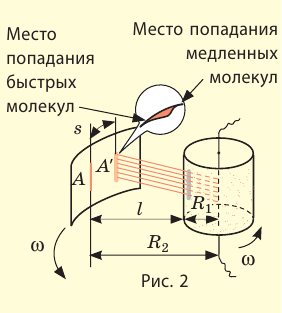
При вращении цилиндров полоска серебра становилась размытой и образовывалась не напротив щели, а на определенном расстоянии s от полоски А (полоска A’). Ведь пока атомы Аргентума проходили расстояние l (см. рис. 2), цилиндры поворачивались. Чем быстрее двигались атомы, тем ближе к полоске А они оседали.
Зная радиусы цилиндров, угловую скорость ω их вращения и измерив расстояние s, Штерн определил скорости v движения атомов Аргентума. Действительно, время движения атомов от щели до внешнего цилиндра равна 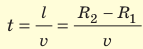
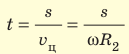
Таким образом, 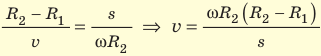
Как и почему взаимодействуют молекулы
Убедиться в том, что молекулы притягиваются друг к другу, достаточно просто. Попробуйте, например, разорвать стальную проволоку или разломить кирпич — это будет сложно, хотя предметы состоят из отдельных частиц. Тот факт, что твердые тела и жидкости не распадаются на отдельные молекулы, превращаясь в газ, тоже говорит о том, что между молекулами существуют силы притяжения. Вместе с тем молекулы отталкиваются друг от друга. В этом легко убедиться, попробовав сжать ту же проволоку или тот же кирпич, — вряд ли вам это удастся.
МКТ утверждает: между молекулами одновременно существуют как силы притяжения, так и силы отталкивания. Основная причина наличия этих сил — электрическое притяжение и отталкивание заряженных частиц, образующих атом: положительно заряженное ядро одного атома притягивается к отрицательно заряженному электронному облаку другого атома; вместе с тем и ядра атомов отталкиваются друг от друга, и электронные облака. Если расстояние r между молекулами меньше размеров d самих молекул (r d) начинают преобладать силы притяжения и молекулы притягиваются друг к другу. Таким образом, на расстоянии r=d молекулы находятся в состоянии устойчивого равновесия: при отклонениях молекулы от этого положения межмолекулярные силы стремятся вернуть ее в состояние равновесия.
При копировании любых материалов с сайта evkova.org обязательна активная ссылка на сайт www.evkova.org
Сайт создан коллективом преподавателей на некоммерческой основе для дополнительного образования молодежи
Сайт пишется, поддерживается и управляется коллективом преподавателей
Whatsapp и логотип whatsapp являются товарными знаками корпорации WhatsApp LLC.
Cайт носит информационный характер и ни при каких условиях не является публичной офертой, которая определяется положениями статьи 437 Гражданского кодекса РФ. Анна Евкова не оказывает никаких услуг.
Движение молекул в физике в газах, жидкостях и твёрдых телах с примерами
Содержание:
Движение молекул:
Почему запах духов распространяется по всей комнате? Могут ли «срастись» два кусочка металла? От чего зависит скорость движения атомов и молекул? На эти и другие вопросы вы сможете ответить, прочитав этот параграф.
Тепловое движение
В соответствии с современными представлениями, атомы и молекулы, из которых состоит вещество, находятся в беспрерывном хаотическом движении. Такое движение называется тепловым.
Тепловое движение невозможно увидеть невооруженным глазом, ведь размеры молекул очень малы.
Однако существует много физических явлений, объяснить которые можно только опираясь на тот факт, что молекулы постоянно двигаются.
Определение диффузии
Бесспорным доказательством движения молекул служит физическое явление, хорошо известное вам из курса природоведения,— диффузия (от лат. diffusio — распространение, растекание).
Напомним, что диффузией называют взаимное проникновение соприкасающихся веществ друг в друга, происходящее в результате теплового (хаотического) движения молекул (атомов).
Диффузия в газах и жидкостях
Вспомните, что происходит, если где-то в комнате разлить ароматное вещество, например духи,— его запах в скором времени будет ощущаться повсюду. Это значит, что молекулы ароматного вещества, двигаясь, попадают в промежутки между молекулами воздуха, которым заполнена комната, т. е. наблюдается диффузия. Именно в результате диффузии в газах мы ощущаем запах свежеиспеченного хлеба из булочной или запах прогретой солнцем травы.
Диффузию можно наблюдать и в жидкостях. Проведем такой опыт. В прозрачный сосуд с чистой водой с помощью воронки нальем раствор медного купороса так, чтобы жидкости не смешались (рис. 2.15). Сначала мы наблюдаем резкую границу между водой и раствором медного купороса. Оставив сосуд в покое на несколько дней, мы увидим, что вся жидкость в сосуде приобрела бирюзовый цвет (рис. 2.16). Причем перемешивание жидкостей произошло без вмешательства извне. Схематически процесс диффузии изображен на рис. 2.17. Многочисленные опыты свидетельствуют, что диффузия в жидкостях протекает значительно медленнее, чем в газах. Еще медленнее происходит диффузия в твердых телах. Почему? Ответ на этот вопрос следует искать в особенностях расположения молекул газов, жидкостей и твердых тел.
Как связаны скорость движения молекул и температура
Приготовим два сосуда, как показано на рис. 2.15. Один из сосудов поставим в теплое место, второй — в холодное. Посмотрев через некоторое время на сосуды, мы убедимся, что в теплом растворе диффузия произошла намного быстрее.
В случае повышения температуры скорость диффузии в газах также увеличивается.
Зависимость скорости диффузии от температуры особенно заметна для твердых тел. Так, английский металлург Вильям Роберт Остин провел следующий опыт. Он наплавил тонкий диск золота на свинцовый цилиндр (рис. 2.18, а) и на несколько дней поместил этот цилиндр в печь, где поддерживалась температура около 400 °С. Оказалось, что золото продиф-фундировало через весь цилиндр (рис. 2.18, б); тем временем при комнатной температуре диффузия практически не наблюдалась.
Таким образом, мы выяснили, что чем выше температура вещества, тем быстрее происходит диффузия, т. е. молекулы быстрее двигаются.
Довольно сложные эксперименты показывают, что при любой температуре в веществе есть молекулы, двигающиеся довольно медленно, и молекулы, скорость которых высока. Если количество молекул вещества, имеющих высокую скорость, увеличивается, т. е. увеличивается средняя скорость молекул, то это значит, что температура вещества также увеличивается.
Диффузия в природа и ее применение в технике
Явление диффузии очень распространено в природе. Благодаря диффузии углекислый газ попадает в листву растений; кислород из воздуха — на дно водохранилищ; питательные вещества впитываются в кишечнике; кислород из легких попадает в кровь, а из крови — в ткани и т. д.
Диффузию широко применяют в технике. Одним из примеров является диффузное сваривание металлов. Куски металлов крепко прижимают друг к другу, нагревают до высокой
температуры, но ниже температуры плавления. В месте соединения происходит диффузия, и куски металлов как будто срастаются.
Атомы и молекулы, из которых состоит вещество, находятся в беспрерывном хаотическом движении. Такое движение называется тепловым, поскольку увеличение температуры вещества соответствует увеличению средней скорости движения его молекул (атомов).
Одним из доказательств движения частиц вещества является физическое явление, которое называется диффузией. Диффузия — взаимное проникновение соприкасающихся веществ друг в друга, происходящее в результате теплового хаотического движения молекул (атомов).
Движение и взаимодействие молекул
Что такое броуновское движение
Броуновское движение — хаотическое движение видимых в микроскоп малых макрочастиц, взвешенных в жидкости или газе, которое происходит под действием ударов молекул.
Это явление названо в честь шотландского ботаника Роберта Броуна (1773–1858), который первым наблюдал его в 1827 г. Рассматривая в микроскоп взвешенные в воде частички пыльцы, Броун заметил, что они непрерывно движутся, постоянно изменяя скорость.
Причина броуновского движения — хаотическое движение молекул жидкости или газа. Двигаясь, молекулы среды непрерывно бомбардируют взвешенную в ней макрочастицу (рис. 27.1). Если суммарная сила ударов с одной стороны случайно окажется больше, чем с другой, то макрочастица может начать движение; потом другие толчки изменят ее скорость.
Теория броуновского движения, созданная А. Эйнштейном и польским физиком M. Смолуховским в 1905–1906 гг. и экспериментально подтвержденная французским физиком Ж. Перреном (рис. 27.2), окончательно закрепила победу атомистики.
Что такое диффузия и где ее применяют
Непрерывное хаотическое движение молекул происходит внутри любого макроскопического тела. В курсе физики 7 класса вы изучали диффузию — еще одно явление, обусловленное таким движением (от лат. diffusio — распространение, растекание).
Диффузия — процесс взаимного проникновения молекул одного вещества между молекулами другого, происходящий вследствие теплового движения молекул.
Если в стакан с водой налить подкрашенный сахарный сироп, спустя некоторое время вода в стакане окрасится и станет сладкой (рис. 27.3, а).
Рис. 27.3. Диффузия в жидкостях и твердых телах. Вследствие теплового хаотического движения молекул сироп смешался с водой в течение суток (а), две отшлифованные и прижатые друг к другу пластины свинца и золота «срослись» на 1 мм в течение 5 лет (б)
Диффузия в жидкости происходит довольно медленно, а в твердых телах она медленнее в сотни и тысячи раз (рис. 27.3). В газах диффузия протекает гораздо быстрее, чем в жидкостях, но все равно: если бы не было конвекции, запах духов распространялся бы в комнате часами. Отметим, что в любых средах скорость диффузии увеличивается с повышением температуры и давления.
Диффузные процессы очень важны для получения и обработки некоторых материалов. Диффузия в твердых телах обеспечивает соединение металлов при сварке, пайке, никелировании. С помощью диффузии поверхностный слой металлических изделий насыщают углеродом, обеспечивая их прочность (рис. 27.4).
Рис. 27.4. Цементация — процесс насыщения поверхностного слоя стали углеродом. если изготовить деталь из низкоуглеродистой стали, а затем поместить ее в высокотемпературную смесь, содержащую углерод, то благодаря диффузии поверхностный слой стали обогатится углеродом. Полученная деталь одновременно будет твердой (снаружи — крепкий чугун) и не будет разрушаться при ударных нагрузках (внутри — упругая сталь)
Разновидностью диффузии является осмос (от греч. osmos — толчок, давление) — процесс односторонней диффузии сквозь полупроницаемую перегородку (мембрану) молекул растворителя в сторону большей концентрации растворенного вещества. Например, если острым ножом отрезать дольку лимона, то сок практически не выделится; если посыпать дольку сахаром, то сок появится. Выделяясь из лимона, сок как бы стремится разбавить концентрированный раствор сахара, образовавшийся на срезе.
В природе благодаря осмосу питательные вещества и вода проникают из почвы в корни растений, из пищеварительного тракта — в организмы живых существ и непосредственно в клетки; кислород из легочных альвеол поступает в кровь и т. п. В промышленности осмос используют для очистки воды, производства напитков, получения некоторых полимеров.
Как быстро движутся молекулы
Молекулы в газах движутся очень быстро — со скоростью пули (см. таблицу), но далеко «улететь» не могут, поскольку ежесекундно испытывают более миллиарда столкновений с другими молекулами. Поэтому траектории движения молекул представляют собой сложные ломаные линии, подобные траектории движения броуновской частицы.
Обратите внимание! В веществе всегда есть молекулы, движущиеся медленно, и молекулы, скорость движения которых огромна. В результате столкновений скорости молекул непрерывно изменяются. Описать движение даже одной молекулы невозможно, да и не нужно. Важно знать, к какому результату приводит движение всей совокупности молекул данного объекта.
Как была измерена скорость движения молекул
Впервые скорость движения молекул измерил немецкий физик Отто Штерн (1888–1969) в 1920 г. Для опыта Штерн изготовил устройство (см. рис. 1), состоящее из двух жестко связанных пустых цилиндров, надетых на общую ось; стенка внутреннего цилиндра имела щель. Вдоль оси была натянута металлическая нить, покрытая слоем серебра. Воздух из цилиндров был откачан. Когда по нитке пропускали ток, серебро испарялось и внутренний цилиндр заполнялся атомами Аргентума, часть которых проходила сквозь щель и оседала на внутренней стенке внешнего цилиндра. В результате напротив щели образовывалась тонкая полоска серебра (А на рис. 2).
При вращении цилиндров полоска серебра становилась размытой и образовывалась не напротив щели, а на определенном расстоянии s от полоски А (полоска A’). Ведь пока атомы Аргентума проходили расстояние l (см. рис. 2), цилиндры поворачивались. Чем быстрее двигались атомы, тем ближе к полоске А они оседали.
Зная радиусы цилиндров, угловую скорость ω их вращения и измерив расстояние s, Штерн определил скорости v движения атомов Аргентума. Действительно, время движения атомов от щели до внешнего цилиндра равна 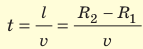
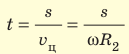
Таким образом, 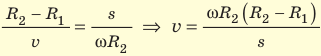
Как и почему взаимодействуют молекулы
Убедиться в том, что молекулы притягиваются друг к другу, достаточно просто. Попробуйте, например, разорвать стальную проволоку или разломить кирпич — это будет сложно, хотя предметы состоят из отдельных частиц. Тот факт, что твердые тела и жидкости не распадаются на отдельные молекулы, превращаясь в газ, тоже говорит о том, что между молекулами существуют силы притяжения. Вместе с тем молекулы отталкиваются друг от друга. В этом легко убедиться, попробовав сжать ту же проволоку или тот же кирпич, — вряд ли вам это удастся.
МКТ утверждает: между молекулами одновременно существуют как силы притяжения, так и силы отталкивания. Основная причина наличия этих сил — электрическое притяжение и отталкивание заряженных частиц, образующих атом: положительно заряженное ядро одного атома притягивается к отрицательно заряженному электронному облаку другого атома; вместе с тем и ядра атомов отталкиваются друг от друга, и электронные облака. Если расстояние r между молекулами меньше размеров d самих молекул (r d) начинают преобладать силы притяжения и молекулы притягиваются друг к другу. Таким образом, на расстоянии r=d молекулы находятся в состоянии устойчивого равновесия: при отклонениях молекулы от этого положения межмолекулярные силы стремятся вернуть ее в состояние равновесия.
При копировании любых материалов с сайта evkova.org обязательна активная ссылка на сайт www.evkova.org
Сайт создан коллективом преподавателей на некоммерческой основе для дополнительного образования молодежи
Сайт пишется, поддерживается и управляется коллективом преподавателей
Whatsapp и логотип whatsapp являются товарными знаками корпорации WhatsApp LLC.
Cайт носит информационный характер и ни при каких условиях не является публичной офертой, которая определяется положениями статьи 437 Гражданского кодекса РФ. Анна Евкова не оказывает никаких услуг.