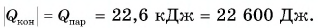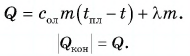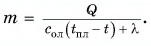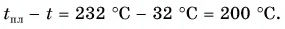От чего зависит кипение воды
Чтобы приготовить различные вкусные блюда, часто необходима вода, и, если ее нагревать, то она рано или поздно закипит. Каждый образованный человек при этом знает, что вода начинает кипеть при температуре, равной ста градусам Цельсия, и при дальнейшем нагревании ее температура не меняется. Именно это свойство воды используется в кулинарии. Однако далеко не всем известно, что это бывает не всегда так. Вода может закипать при разной температуре в зависимости от условий, в которых она находится. Давайте попробуем разобраться, от чего зависит температура кипения воды, и как это нужно использовать.
При нагревании температура воды приближается к температуре кипения, и по всему объему образуются многочисленные пузырьки, внутри которых находится водяной пар. Плотность пара меньше, чем плотность воды, поэтому сила Архимеда, действующая на пузырьки, поднимает их на поверхность. При этом объем пузырьков то увеличивается, то уменьшается, поэтому закипающая вода издает характерные звуки. Достигая поверхности, пузырьки с водяным паром лопаются, по этой причине кипящая вода интенсивно булькает, выпуская водяной пар.
Температура кипения в явном виде зависит от давления, оказываемого на поверхность воды, что объясняется зависимостью давления насыщенного пара, находящегося в пузырьках, от температуры. При этом количество пара внутри пузырьков, а вместе с этим и их объем, увеличиваются до тех пор, пока давление насыщенного пара не будет превосходить давление воды. Это давление складывается из гидростатического давления воды, обусловленного гравитационным притяжением к Земле, и внешнего атмосферного давления. Поэтому температура кипения воды увеличивается при возрастании атмосферного давления и уменьшается при его уменьшении. Только в случае нормального атмосферного давления 760 мм.рт.ст. (1 атм.) вода кипит при 100 0 С. График зависимости температуры кипения воды от атмосферного давления представлен ниже:
Из графика видно, что если увеличить атмосферное давление до 1,45 атм, то вода будет кипеть уже при 110 0 С. При давлении воздуха 2,0 атм. вода закипит при 120 0 С и так далее. Увеличение температуры кипения воды может быть использовано для ускорения и улучшения процесса приготовления горячих блюд. Для этого изобрели скороварки – кастрюли с особой герметично закрывающейся крышкой, снабженные специальными клапанами для регулирования температуры кипения. Из-за герметичности давление в них повышается до 2-3 атм., что обеспечивает температуру кипения воды 120-130 0 С. Однако при этом нужно помнить, что использование скороварок сопряжено с опасностью: пар, выходящий из них, имеет большое давление и высокую температуру. Поэтому нужно быть максимально осторожными, чтобы не получить ожог.
Обратный эффект наблюдается, если атмосферное давление понижается. В этом случае температура кипения тоже уменьшается, что и происходит при увеличении высоты над уровнем моря:
ОПРЕДЕЛЕНИЕ ТЕМПЕРАТУРЫ КИПЕНИЯ
Каждая чистая жидкость кипит при вполне определенной постоянной температуре, зависящей от внешнего давления. Таким образом, постоянство температуры кипения жидкости может служить* критерием ее чистоты. Если высушенная жидкость при определенном давлении (нормальном или пониженном) полностью перегоняется при температуре, указанной в справочнике, то с известным основанием можно утверждать, что она является химически чистой. В противном случае жидкость чем-то загрязнена.
В лабораторной практике часто приходится определять температуру кипения жидкостей. Самым простым прибором для определения температуры кипения является прибор, изображенный на рис. 499. Это — круглодонная колба 1, имеющая широкое горло. Последнее закрывают пробкой, в которую вставлены термометр 2 и согнутая трубка 3. Емкость колбы 1 должна быть не менее 50 мл. Жидкость, температуру кипения которой нужно определить, наливают в количестве, равном приблизительно 1/4 объема колбы. При определении температуры кипения чистой жидкости резервуар термометра находится па небольшом расстоянии от поверхности жидкости и не должен касаться ее. Если определяют температуру кипения раствора, то резервуар термометра опускают в жидкость. Образующиеся пары жидкости уходят через изогнутую трубку 3, которую можно соединить с холодильником.
Если температура кипения жидкости не выше 90° С, то нагревать ее лучше всего на водяной бане. Если температура кипения выше 90° С, то нагревать можно при помощи маленькой газовой горелки или электрической воронкообразной печи (колбонагревателя).
* Следует иметь в виду, что жидкие азеотроппые смеси также кипят при постоянной температуре.
Наблюдения за показаниями термометра следует вести в течение не менее 15 мин и считать температурой кипения ту, которую будет показывать установившийся столбик ртути. Если взята чистая жидкость, постоянная температура кипения устанавливается быстро; если же жидкость содержит какие-либо примеси, температура кипения будет изменяться. Так как все температуры кипения, указываемые в справочниках, относятся к нормальному давлению (760 мм рт. ст.), то полученную температуру кипения также следует привести к этому давлению. Поэтому одновременно с показаниями термометра следует обязательно отмечать атмосферное давление по барометру и запись вести, например, так:
На основании этих данных вычисляют температуру кипения жидкости при 760 мм рт. ст. Для многих жидкостей в справочниках есть таблицы поправок температур кипения при разных давлениях для приведения их к 760 мм рт. ст.
Если же таблиц нет, то можно вычислить вероятную поправку, так как температура кипения многих жидкостей при 760 мм рт. ст. изменяется приблизительно одинаково— на 0,038° С (или 3/80) с изменением давления на 1 мм рт. ст. Если давление B, определяемое по барометру, меньше 760 мм рт. ст., то к наблюдавшейся температуре кипения следует прибавить величину, получаемую из формулы:

Если давление выше-, то вычитают величину, получаемую из формулы:

Кроме указанного прибора, требующего довольно большого объема жидкости, имеется ряд других, которые дают возможность работать с небольшими количествами ее (от 1 до 5 мл).
Аппарат, изображенный иа рис. 500, состоит из сосуда 1 диаметром 35 мм и длиной 170 мм; в него на пробке вставляют другой сосуд 2 диаметром 18 мм и длиной 170 мм. В середине этого сосуда имеется боковая загнутая внутрь трубка 3, доходящая почти до дна сосуда 2. Термометр 4 вставляют на пробке в сосуд 2 до дна его.

Для определения точки кипения в этом приборе наливают 3—5 мл жидкости в сосуд 1 и нагревают голым пламенем. Для равномерного кипения в жидкость полезно добавить 0,2—0,3 г пемзы зернами диаметром 1 мм, предварительно хорошо прокипяченной с разбавленной HCl, промытой и прокаленной. Образующиеся пары жидкости через трубку 3 поступают в сосуд 2 и выходят из него через отводную трубку 5.
Прибор очень удобен в работе и дает хорошие результаты. В особенности этот прибор пригоден для жидкостей и твердых тел с высокой температурой кипения (выше 300°С).
Если имеется всего несколько капель жидкости, ее температуру кипения можно определять при помощи прибора Сиволобова. Прибор представляет собой стеклянную трубку длиной около 100 мм и внутренним диаметром около 5—6 мм, один конец которой сужен почти вдвое и запаян. Длина суженного конца около 10 мм. При помощи капиллярной пипетки узкую часть трубки заполняют теплоносителем. В жидкость опускают запаянный с одного конца очень тонкий стеклянный капилляр такой же длины, как и основная трубка, в ка-: пилляр наливают несколько капель определяемой жидкости. К термометру прикрепляют трубку с капилляром и опускают в прибор для определения температуры кипения. Когда при нагревании температура жидкости будет близка к температуре кипения, нз капилляра начинают выделяться отдельные воздушные пузырьки. Когда будет достигнута температура кипения, из капилляра через жидкость проходит равномерный ток пузырьков. При повторении определения температуры кипения капилляр в приборе заменяют другим.
О приборах для определения температуры кипения см. M и« х а и л о в Л. А.. Парташннкова М. 3., Зав. лаб., 23, № II, 1338 (1957); Lykos P. G., Chem. Educ, 35, Ks 11, 565 (1958).
Вайсбергер А., Физические методы органической химии, т. 1, Издатинлпт, 1950; Вейганд K-, Методы эксперимента в органичен скои химии, т. 1, Издатннлит, 1950; Черонис H., Микро- и полу* микрометоды органической химии, Издатинлит, 1960.
О микрометоде определения температуры кипения см. BoIi-1п е H., В ohm R. H., Mikrochim. Acta, Ki 2, 270 (1959); РЖХим, 1959, Ki 21, 157, реф. 74745.
Молекулярная физика. Кипение жидкости.
Кипение — это интенсивный переход жидкости в пар, происходящий с образованием пузырьков пара по всему объему жидкости при определенной температуре.
В отличие от испарения, которое происходит при любой температуре жидкости, другой вид парообразования — кипение — возможен лишь при совершенно определенной (при данном давлении) температуре — температуре кипения.
При нагревании воды в открытом стеклянном сосуде можно увидеть, что по мере увеличения температуры стенки и дно сосуда покрываются мелкими пузырьками. Они образуются в результате расширения мельчайших пузырьков воздуха, которые существуют в углублениях и микротрещинах не полностью смачиваемых стенок сосуда.
Пары жидкости, которые находятся внутри пузырьков, являются насыщенными. С ростом температуры давление насыщенных паров возрастает, и пузырьки увеличиваются в размерах. С увеличением объема пузырьков растет и действующая на них выталкивающая (архимедова) сила. Под действием этой силы наиболее крупные пузырьки отрываются от стенок сосуда и поднимаются вверх. Если верхние слои воды еще не успели нагреться до 100 °С, то в такой (более холодной) воде часть водяного пара внутри пузырьков конденсируется и уходит в воду; пузырьки при этом сокращаются в размерах, и сила тяжести заставляет их снова опускаться вниз. Здесь они опять увеличиваются и вновь начинают всплывать вверх. Попеременное увеличение и уменьшение пузырьков внутри воды сопровождается возникновением в ней характерных звуковых волн: закипающая вода шумит.
Когда вся вода прогреется до 100 °С, поднявшиеся вверх пузырьки уже не сокращаются в размерах, а лопаются на поверхности воды, выбрасывая пар наружу. Возникает характерное бульканье — вода кипит.
Кипение начинается после того, как давление насыщенного пара внутри пузырьков сравнивается с давлением в окружающей жидкости.
Во время кипения температура жидкости и пара над ней не меняется. Она сохраняется неизменной до тех пор, пока вся жидкость не выкипит. Это происходит потому, что вся подводимая к жидкости энергия уходит на превращение ее в пар.
Температура, при которой кипит жидкость, называется температурой кипения.
Температура кипения зависит от давления, оказываемого на свободную поверхность жидкости. Это объясняется зависимостью давления насыщенного пара от температуры. Пузырек пара растет, пока давление насыщенного пара внутри него немного превосходит давление в жидкости, которое складывается из внешнего давления и гидростатического давления столба жидкости.
Чем больше внешнее давление, тем больше температура кипения.
Всем известно, что вода кипит при температуре 100 ºC. Но не следует забывать, что это справедливо лишь при нормальном атмосферном давлении (примерно 101 кПа). При увеличении давления температура кипения воды возрастает. Так, например, в кастрюлях-скороварках пищу варят под давлением около 200 кПа. Температура кипения воды при этом достигает 120°С. В воде такой температуры процесс варки происходит значительно быстрее, чем в обычном кипятке. Этим и объясняется название «скороварка».
И наоборот, уменьшая внешнее давление, мы тем самым понижаем температуру кипения. Например, в горных районах (на высоте 3 км, где давление составляет 70 кПа) вода кипит при температуре 90 °С. Поэтому жителям этих районов, использующим такой кипяток, требуется значительно больше времени для приготовления пищи, чем жителям равнин. А сварить в этом кипятке, например, куриное яйцо вообще невозможно, так как при температуре ниже 100 °С белок не сворачивается.
У каждой жидкости своя температура кипения, которая зависит от давления насыщенного пара. Чем выше давление насыщенного пара, тем ниже температура кипения соответствующей жидкости, т. к. при меньших температурах давление насыщенного пара становится равным атмосферному. Например, при температуре кипения 100 °С давление насыщенных паров воды равно 101 325 Па (760 мм рт. ст.), а паров ртути — всего лишь 117 Па (0,88 мм рт. ст.). Кипит ртуть при 357°С при нормальном давлении.
Теплота парообразования.
Теплота парообразования (теплота испарения) — количество теплоты, которое необходимо сообщить веществу (при постоянном давлении и постоянной температуре) для полного превращения жидкого вещества в пар.
Физическая величина, показывающая, какое количество теплоты необходимо, чтобы обратить жидкость массой 1 кг в пар без изменения температуры, называется удельной теплотой парообразования.
Удельную теплоту парообразования обозначают буквой r и измеряют в джоулях на килограмм (Дж/кг).
Количество теплоты, необходимое для парообразования (или выделяющееся при конденсации). Чтобы вычислить количество теплоты Q, необходимое для превращения в пар жидкости любой массы, взятой при температуре кипения, нужно удельную теплоту парообразования r умножить на массу m:
При конденсации пара происходит выделение такого же количества теплоты:
Содержание:
Кипение жидкостей:
Вы уже знаете, что испарение жидкости без притока теплоты при любой температуре приводит к ее охлаждению. А как будет идти испарение, если жидкости непрерывно передавать энергию (теплоту)?
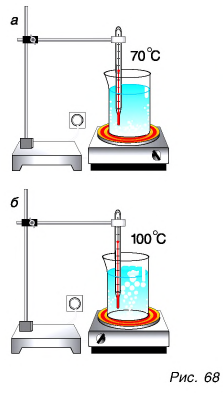
Проведем опыт. Поставим на электроплитку стакан с водой (рис. 68, а). По термометру будем следить за изменением температуры воды в стакане. Температура воды сначала растет. На дне стакана появляется множество маленьких пузырьков. Их размеры постепенно увеличиваются, так как вода испаряется внутрь пузырьков и давление пара в пузырьках при нагревании повышается. Пузырьки отрываются ото дна и стенок и движутся вверх. А что дальше? Если давление пара внутри пузырька больше, чем над жидкостью, то у поверхности он разрывается, и пар выходит наружу. При этом температура воды близка к 100 °C и практически не меняется. А все большее число пузырьков поднимается и лопается у поверхности, выбрасывая пар в атмосферу. Вода кипит (рис. 68, б).
Что такое кипение
Кипение — это процесс парообразования, идущий при постоянной температуре но всему объему жидкости. Действительно, любой пузырек можно рассматривать как сосуд с паром внутри жидкости (рис. 69). С поверхности его стенок идет испарение и обратный процесс — возврат молекул в жидкость, т. е. конденсация.
При кипении температура жидкости не меняется. По ведь энергия (от нагретой плитки) жидкостью поглощается. На что же она расходуется? Энергия, полученная жидкостью, идет на превращение ее в пар (газ), т. е. на преодоление сил притяжения между молекулами жидкости.
При обратном процессе — переходе пара в жидкость (рис. 70), или конденсации, это же количество энергии выделяется.
Температура, при которой происходит кипение жидкости, называется температурой кипения.
Температура кипения у разных жидкостей неодинакова. Это и понятно, ведь энергия взаимодействия их молекул тоже разная.
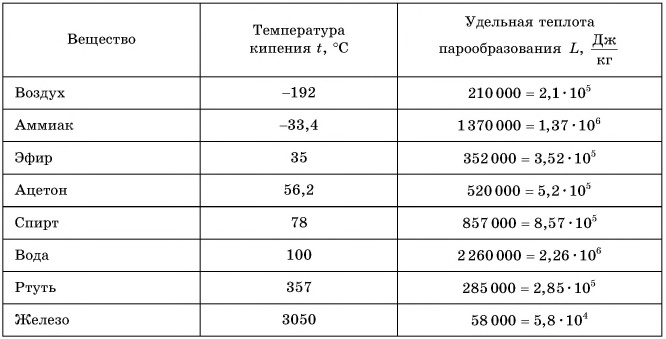
В таблице 4 приведены температуры кипения жидкостей при нормальном атмосферном давлении.
А случайно ли мы, говоря о температуре кипения жидкости, указываем давление? Нет, не случайно. Пузырьки кипящей жидкости лопаются при условии, что давление пара в них не меньше, чем давление снаружи. Значит, чем меньше внешнее давление, тем при более низкой температуре закипит жидкость.
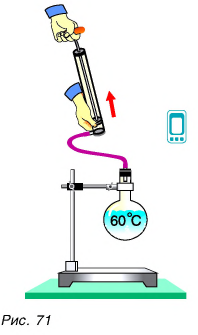
Подтвердим это опытом. Нальем в колбу теплой воды, температура которой t = 50—60 °C. Закроем колбу пробкой, подсоединенной к откачивающему насосу (рис. 71). Откачаем газ из колбы. Вода закипит, хотя ее температура меньше 100 °C. Ио это не значит, что в такой воде можно сварить яйцо. Яйцо варится не потому, что вода кипит, а потому, что она горячая.
А если в специальных условиях создать высокое давление над поверхностью воды, то в ней можно будет расплавить олово, но вода так и не будет кипеть. Объясните почему.
Зависимость температуры кипения от внешнего давления используется в практических целях. Например, для стерилизации медицинских инструментов их помещают в герметически закрытые камеры-автоклавы (рис. 72), вода в которых кипит при температуре значительно выше 100 °C. В быту используются кастрюли-скороварки (рис. 73), в которых температура кипения воды может повышаться до 120 °C. Поэтому пища в скороварках готовится гораздо быстрее, чем в обычных кастрюлях.
Вернемся к парообразованию. Чтобы превратить в пар 1 кг жидкости при температуре кипения, необходимо передать ей определенное количество теплоты. А если масса жидкости будет 2 кг? Значит, теплоты понадобится в 2 раза больше. А при превращении в пар m кг жидкости количество теплоты увеличится в m раз, т. е. количество теплоты, необходимое для парообразования, прямо пропорционально массе жидкости:
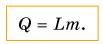
В этой формуле коэффициент L называется удельной теплотой парообразования: 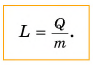
Как следует из формулы, единицей удельной теплоты парообразования в СИ является 1 джоуль на килограмм
Удельная теплота парообразования есть физическая величина, численно равная количеству теплоты, поглощенному 1 кг жидкости при переходе ее в пар при температуре кипения.
Таблица 4. Температура кипения и удельная теплота парообразования некоторых жидкостей (при нормальном атмосферном давлении)
Удельная теплота парообразования различных жидкостей дана в таблице 4. Что значит 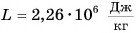
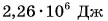
Можно сказать и иначе: 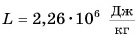
Главные выводы:
Пример решения задачи
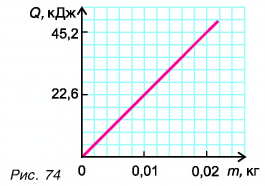
На рисунке 74 представлен график зависимости количества теплоты, идущего на парообразование некоторой жидкости, от ее массы. Какую массу олова можно расплавить, используя теплоту конденсации пара данной жидкости массой 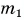
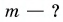
Решение
Из графика найдем модуль количества теплоты, которое выделится при конденсации пара массой 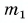
Для нагревания до температуры плавления 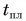
Откуда
Тогда
При копировании любых материалов с сайта evkova.org обязательна активная ссылка на сайт www.evkova.org
Сайт создан коллективом преподавателей на некоммерческой основе для дополнительного образования молодежи
Сайт пишется, поддерживается и управляется коллективом преподавателей
Whatsapp и логотип whatsapp являются товарными знаками корпорации WhatsApp LLC.
Cайт носит информационный характер и ни при каких условиях не является публичной офертой, которая определяется положениями статьи 437 Гражданского кодекса РФ. Анна Евкова не оказывает никаких услуг.
Кипение
Содержание
Для того чтобы превратить жидкость в пар, существует два способа: испарение и кипение. В прошлых уроках мы подробно разобрали, как происходит процесс испарения. В его ходе образуется пар, который в зависимости от условий может быть насыщенным или ненасыщенным.
Явление кипения мы часто наблюдаем в повседневной жизни. Для того чтобы приготовить чай или кофе, сначала мы доводим воду до кипения. Чтобы сварить суп, мы ждем, когда закипит вода в кастрюле.
В данном уроке мы рассмотрим, как физика описывает этот процесс, изучим изменения, происходящие при кипении и установим зависимости от других величин.
Процесс кипения
Проведем опыт: будем нагревать воду в открытом стеклянном сосуде и измерять ее температуру.
Отметим, что до того, момента как мы начнем нагревать воду, с поверхности воды идет испарение. Пар при этом не виден глазу, но, тем не менее, существует.
Начнем нагревать воду. Мы заметим, что в воде начинают появляться пузырьки (рисунок 1, а). С повышением температуры они начинают увеличиваться в размерах.
В воде всегда растворено некоторое количество воздуха. При повышении температуры этот воздух выделяется из воды в виде пузырьков. Внутри них – воздух и водяной пар. Водяной пар там присутствует, потому что окружающая вода испаряется внутрь этих пузырьков воздуха.
Когда пузырьки поднимаются в верхние слои жидкости (более холодные), они уменьшаются в размерах. Происходит это из-за конденсации пара внутри пузырьков. Под действием силы тяжести они опускаются вниз в более горячую воду.
И снова начинают подниматься к поверхности. Происходит попеременное увеличение и уменьшение пузырьков, в ходе которых они двигаются в жидкости. При этом мы слышим шум. Он предшествует закипанию воды.
Кипение – это интенсивный переход жидкости в пар, происходящий с образованием пузырьков пара по всему объему жидкости при определенной температуре.
Температура кипения
Если испарение происходит при любой температуре, то кипение происходит при некоторой определенной температуре. При этом:
Температура кипения – это температура, при которой жидкость кипит.
Во время кипения температура жидкости не меняется.
Вспомните, при приготовлении того же супа после закипания воды огонь уменьшают. Теперь он просто поддерживает эту самую температуру кипения. Это дает экономию топлива.
Температура кипения зависит от давления на поверхность жидкости. Давление насыщенного пара в пузырьках при кипении всегда больше внешнего давления.
Соответственно, если мы увеличим внешнее давление, то температура кипения увеличивается. Если уменьшим – температура кипения тоже снизится.
Температура кипения некоторых веществ
В таблице 1 представлены экспериментально полученные значения температуры кипения для различных веществ.
| Вещество | $t_<кип>, \degree C$ | Вещество | $t_<кип>, \degree C$ |
| Водород | -253 | Вода | 100 |
| Кислород | -183 | Ртуть | 357 |
| Эфир | 35 | Свинец | 1740 |
| Спирт | 78 | Медь | 2567 |
| Молоко | 100 | Железо | 2750 |
Талица 1. Температура кипения некоторых веществ (при нормальном атмосферном давлении)
Графики кипения жидкостей
На рисунке видно, что горизонтальные участки графиков соответствуют процессам кипения. Они параллельны оси времени, температура на них остается постоянной. Чтобы определить, какой график соответствует каждой жидкости, нам нужно обратиться к таблице 1.
$70 \degree C$ – температура кипения спирта. Значит, 2 – график нагревания и кипения спирта.